
Глюкозодегидрогеназа (ГДГ)
Описание
Глутаматдегидрогеназа (ГДГ) представляет собой митохондриальный фермент, который катализирует обратимое окислительное дезаминирование глутамата до α-кетоглутарата и служит ключевым связующим звеном между анаболическими и катаболическими путями.У млекопитающих ГДГ подвергается аллостерической регуляции и обладает высокой активностью в печени, почках, головном мозге и поджелудочной железе.Активность ГДГ в сыворотке можно использовать для дифференциации заболеваний печени, вызванных воспалением печени, при которых не наблюдается повышенной активности ГДГ в сыворотке, и заболеваний, которые приводят к некрозу гепатоцитов, что приводит к повышению уровня ГДГ в сыворотке.
Активность GDH определяют с помощью связанного ферментативного анализа, в котором глутамат поглощается GDH, образуя NADH, который реагирует с зондом, образуя колориметрический (450 нм) продукт, пропорциональный присутствующей активности GDH.Одна единица GDH – это количество фермента, которое будет генерировать 1,0 ммоль NADH в минуту при pH 7,6 при 37 °C.
Химическая структура
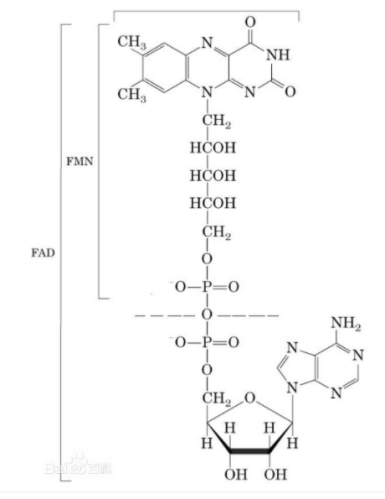
Механизм реакции
D-глюкоза + акцептор → D-глюконо-1,5-лактон + восстановленный акцептор
Спецификация
| Тестовые задания | Технические характеристики |
| Описание | Белый аморфный порошок, лиофилизированный |
| Активность | ≥160U/мг |
| Чистота (SDS-СТРАНИЦА) | ≥90% |
| Растворимость (10 мг порошка/мл) | Прозрачный |
| Загрязняющие ферменты | |
| Глюкозодегидрогеназа (НАД) | ≤0,02% |
| гексокиназа | ≤0,02% |
| А-глюкозидаза | ≤0,02% |
Транспортировка и хранение
Транспорт: Пакеты со льдом
Хранилище :Хранить при температуре от -25 до -15 °C (длительно), от 2 до 8 °C (кратковременно).
Рекомендуемое повторное тестированиеЖизнь: 18 месяцев














